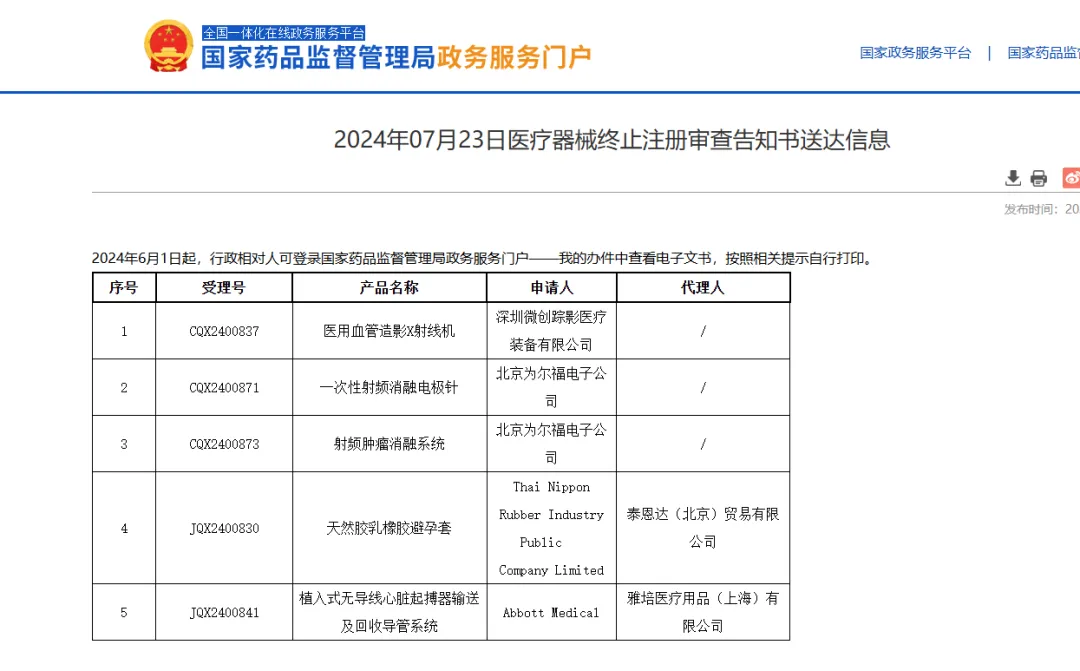
近日,根据国家药品监督管理局(NMPA)发布的医疗器械终止注册审查告知书送达信息,国际医疗器械巨头雅培医疗用品(上海)有限公司的一款高风险医疗器械——植入式无导线心脏起搏器输送及回收导管系统,其注册申请已被终止。该告知书编号为JQX2400841,发布于2024年7月23日,标志着这款产品在中国的注册进程遭遇了重大变化。
据悉,自2024年6月1日起,行政相对人可通过国家药品监督管理局政务服务门户查询相关电子文书,并按照提示自行打印。此次终止注册的医疗器械,作为高风险类别,其在医疗领域的应用广泛且重要,通常对技术、安全性和疗效有极高的要求。
雅培医疗用品(上海)有限公司作为全球知名的医疗设备制造商,其产品在市场上享有较高的声誉。然而,此次植入式无导线心脏起搏器输送及回收导管系统的注册终止,无疑给其在中国市场的布局带来了一定的不确定性。具体原因虽未明确公布,但可能涉及技术评估、安全审核或市场策略调整等多个方面。
值得注意的是,医疗器械的注册过程复杂且严格,需要经历多轮评审和验证。此次终止注册,可能是基于对产品性能、安全性或符合性标准的全面考量。对于雅培来说,面对这一挑战,未来可能需要重新评估和调整其在中国市场的产品策略,以确保满足监管要求和市场需求。
此次事件也再次提醒我们,医疗器械的安全性和有效性对于患者至关重要。在全球化日益加深的今天,各国监管部门正不断加强合作与沟通,共同推动医疗器械行业的健康发展。同时,对于医疗器械生产企业而言,严格遵守监管规定、不断提升产品质量和技术水平,将是其赢得市场认可和信任的关键所在。
一纸通告几个字,浇灭的是申办方多年的积累,费尽心思多年做出来的产品不一定符合中国的要求。所以医疗器械投资,尤其是高风险医疗器械的投资,风险巨大,当然成功了,收益也是非常巨大的。
鸿盟医学
医疗器械全球注册咨询、医疗器械临床试验、医疗器械质量管理体系(ISO13485/GMP/QSR)、医疗器械可用性研究、
医疗器械法规培训为一体的专业技术咨询服务机构
微信号:hom_medical、18018710006 联系电话:18018716006
 鸿盟标准技术(深圳有限公司)
鸿盟标准技术(深圳有限公司)